USZKODZENIE WIĘZADŁA KRZYŻOWEGO PRZEDNIEGO (ACL).
WSTĘP
W ostatnich latach można zaobserwować znaczący wzrost zainteresowania aktywnym trybem życia oraz zwiększenie liczby osób amatorsko uprawiających sport w różnym przedziale wiekowym. Taka tendencja, wraz z niskim stopniem świadomości dotyczącej kultury fizycznej, powoduje zwiększenie częstości występowania mikrourazów narządu ruchu, a w przypadku długotrwałego sumowania się ich w czasie mogą one doprowadzić nawet do poważniejszych uszkodzeń.
Wiele prac naukowych podejmuje problematykę uszkodzenia więzadła krzyżowego przedniego (ACL), gdyż stanowi ono istotny odsetek wśród urazów narządu ruchu. Występowanie urazu ACL wynosi około 1/3000 uszkodzeń więzadłowych stawu kolanowego w skali światowej.
Omawiany problem dotyczy zarówno osób trenujących wyczynowo, rekreacyjnie, jak i tych niezwiązanych z aktywnością sportową. Najczęściej do urazu dochodzi w sposób pośredni; na przykład podczas zeskoku, gwałtownego manewru omijającego przeszkodę czy nagłego zatrzymania się. Dlatego też badacze często wymieniają sporty takie jak koszykówka, siatkówka, piłka nożna, narciarstwo jako aktywności, w których najczęściej może dojść do uszkodzenia więzadła krzyżowego przedniego.
Z biomechanicznego punktu widzenia więzadło to jest główną strukturą pasywną ograniczającą translację kości piszczelowej w przód (anterior tibial translation- ATT) względem kości udowej. Ponadto ACL odgrywa ważną rolę w stabilizacji rotacyjnej stawu kolanowego, a jego uszkodzenie często objawia się poczuciem niestabilności, co może przyczynić się do zmiany biomechanicznego obrazu chodu. W długotrwałych zaś skutkach nieleczone zerwanie ACL może doprowadzić do powstania zmian degeneracyjnych chrząstki stawowej, na skutek zwiększonej ruchomości partnerów stawowych względem siebie. Może doprowadzić to do nasilenia się dolegliwości bólowych, a w konsekwencji do ograniczenia, a nawet do zaprzestania aktywności fizycznej.
W poniższym artykule chciałbym omówić kilka zagadnień związanych z tematem uszkodzenia ACL, takich jak:
- etiologia i czynniki ryzyka,
- diagnostyka i metody leczenia,
- rehabilitacja.
ETIOLOGIA I CZYNNIKI RYZYKA
Najprościej tłumacząc; do uszkodzenia ACL dochodzi, gdy napięcie wiązadła jest na tyle duże, że przekracza ono jego naturalną wytrzymałość. Najczęściej uraz powstaje w sposób pośredni (non-contact), kiedy to obie stopy mają kontakt z podłożem w warunkach obciążenia kończyn dolnych. Dzięki dostępnym pracom naukowym można zauważyć, że problem uszkodzenia ACL dotyczy w przeważającej ilości młodszej populacji.
Jest ono również jednym z najczęstszych urazów w sporcie oraz w przeważającej ilości u płci żeńskiej ze względu na:
-
różnice hormonalne, głównie związane z poziomem estrogenu,
-
odmienną budowę morfologiczną stawu kolanowego,
-
większą tendencję do koślawienia kolan szczególnie podczas zeskoku,
-
generowanie większych sił ścinających w kolanie.
Powyższe czynniki oraz dysproporcję międzypłciową w częstotliwości wystąpienia urazu ACL można zaobserwować głównie na początku okresu pokwitania.
Obecnie coraz lepiej poznane są czynniki predysponujące do urazu więzadła krzyżowego przedniego w sposób pośredni. Najczęściej wymienianymi i powtarzającymi się w literaturze są:
-
mały kąt zgięcia lub przeprost kolana,
-
duża siła reakcji podłoża o kierunku tylnym,
-
koślawość kolana połączona z rotacją zewnętrzną lub wewnętrzną,
-
obecność dużych sił ścinających w obrębie stawu kolanowego skierowanych do przodu,
-
zwiększona wiotkość struktur okołostawowych, powodująca jego nadmierną ruchomość.
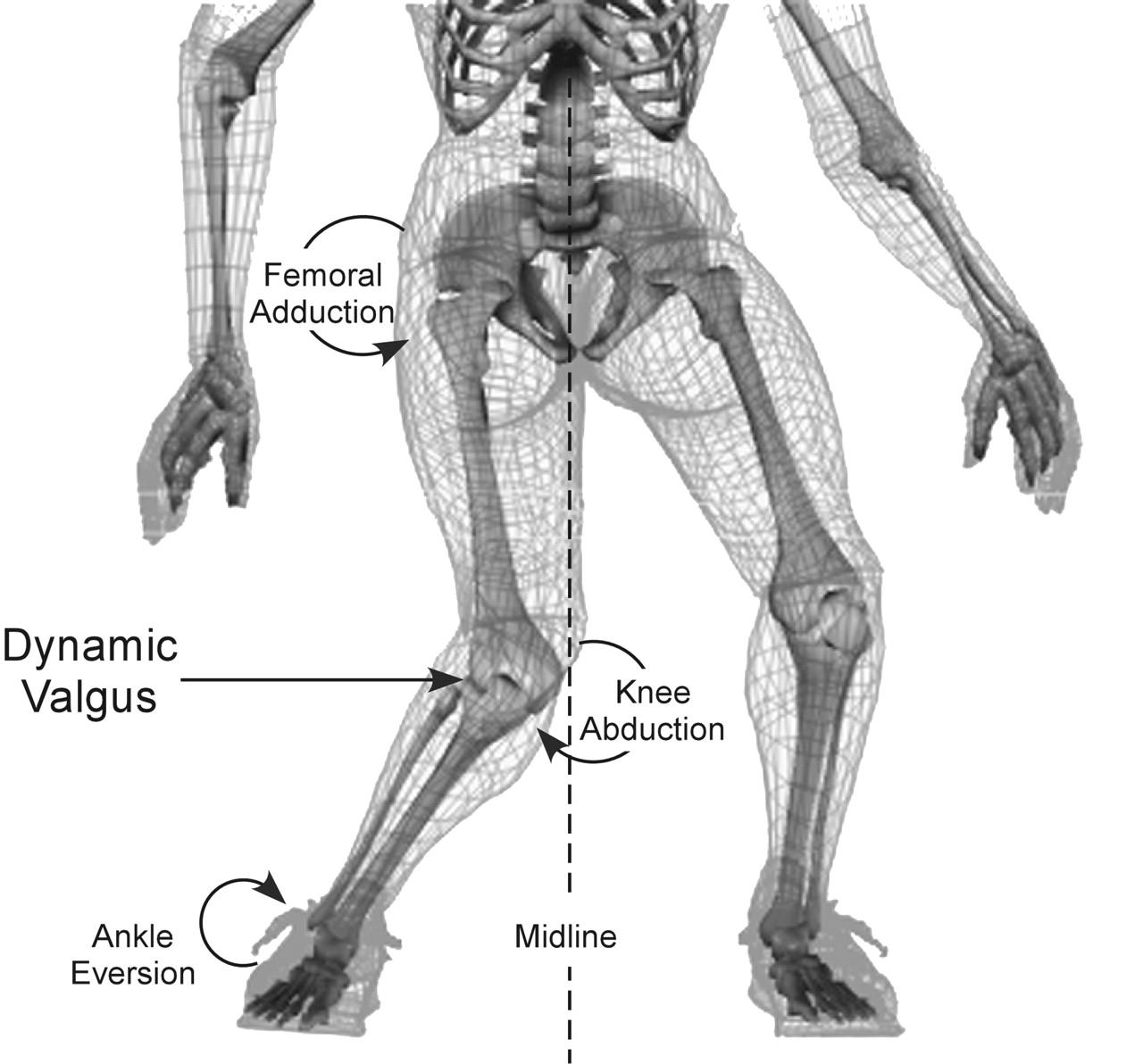
Ryc.1. Czynniki ryzyka uszkodzenia ACL. Na powyższej projekcji komputerowej przedstawiono typowe czynniki ryzyka uszkodzenia wiązania krzyżowego przedniego związane z pozycją kończyny dolnej. Oznaczono na niej przywiedzenie kości udowej oraz kolana przy ustabilizowanej stopie, czego wynikiem jest wystąpienie dynamicznej koślawości. Występuje również ewersja w stawie skokowym czemu może towarzyszyć rotacja zewnętrzna podudzia. Opisane powyżej czynniki powodują powstanie wysokiego napięcia w obrębie ACL, efektem czego może dojść do jego uszkodzenia.
Najczęściej wymienianymi aktywnościami, podczas których dochodzi do wywołania większości z powyższych czynników uszkodzenia ACL są lądowanie po wyskoku czyli zeskok oraz nagła zmiana kierunku ruchu. Dlatego uraz ten najczęściej występuje podczas uprawiania sportu o wysokiej intensywności. W literaturze często grupy badawcze stanowią osoby ćwiczące piłkę nożną oraz ręczną, koszykówkę, rugby, sporty kontaktowe czy narciarstwo.
DIAGNOSTYKA I METODY LECZENIA
Do oceny uszkodzenia ACL najczęściej stosowane są testy diagnostyczne, które w przypadku wątpliwości potwierdzane są poprzez badanie rezonansem magnetycznym (MRI), rzadziej tomografią komputerową (CT).
Większość (blisko 80%) urazów ACL jest całkowite, dlatego też przy podejrzeniu ich uszkodzenia wykonuje się najczęściej następujące testy kliniczne:
-
Test Lachmanna,
-
Test Przedniej Szuflady,
-
Test Pivot-Shift.
Trzeba jednak podkreślić, że skuteczność wyżej wymienionych testów w przypadku stanu ostrego urazu ACL jest niska ze względu na ból i możliwą opuchliznę, która ogranicza możliwości diagnostyczne. Dlatego czułość powyższych testów przedstawia się następująco:
-
84 – 98,4% skuteczności diagnostycznej w stanach przewlekłej niewydolności
ACL, gdzie dochodzi do występowania znacznej niestabilności; -
35% skuteczności diagnostycznej w stanach ostrych zerwania ACL;
-
98,4% skuteczności u pacjentów znieczulonych ze zerwaniem ACL.
W związku z tym bardzo pomocna jest diagnostyka obrazowa jaką zapewnia MRI, za pomocą którego można precyzyjnie określić rozległość urazu ACL. Rzadko kiedy stosuje się CT ponieważ potwierdza ona jedynie zerwanie ACL powstałe w sposób awulsyjny.
Pomimo dużej ilości publikacji naukowych tłumaczących zjawisko zerwania ACL, nie ma jednoznacznego stanowiska odnośnie wyboru sposobu leczenia. Obecnie przedstawia się dwa fronty podejścia do uszkodzenia ACL. Jeden stanowi nieoperacyjne, zachowawcze leczenie, a drugi rekonstrukcyjne odtworzenia ACL poprzez przeszczep, najczęściej autogeniczny, ze ścięgna rzepki bądź mięśnia półścięgnistego. Z jednej strony dobrze przeprowadzone badania udokumentowały potencjalnie niższą częstotliwość występowania uszkodzeń łąkotek lub degeneracji chrząstki stawowej po operacyjnym leczeniu ACL, z drugiej zaś wykazały one zwiększone ryzyko wtórnej osteoartrozy (OA) w przeciągu 10 lat od zabiegu.
Najczęściej rekonstrukcję ACL wykonuje się u ”młodych dorosłych”, osób aktywnych fizycznie czy sportowców, których celem jest powrót do rywalizacji na najwyższym poziomie. Farshad i wsp. poprzez analizę i zestawienie dostępnej literatury naukowej wyodrębnili dwie grupy badawcze. Jedna z nich była leczona operacyjnie (229 osób), zaś druga (155 osób) zachowawczo. Zauważono, że proporcja pacjentów, którzy powrócili do aktywności fizycznej na wysokim poziomie była znacząco wyższa w grupie leczonej operacyjnie (70,7%), niż w przypadku grupy leczonej zachowawczo (49,7%).
Obecne badania wskazują, że powrót do aktywności fizycznej jest podobny w obu grupach leczonych zarówno operacyjnie jak i zachowawczo. Odsetek osób, które poddają się rekonstrukcji ACL pomimo leczenia zachowawczego nie przekracza 30%. Trzeba jednak zaznaczyć, że stan wyjściowy takich osób jest znacznie lepszy niż osób operowanych świeżo po urazie, a powrót do aktywności fizycznej jest znacznie szybszy. Jest to rezultatem leczenia zachowawczego – rehabilitacji – po zerwaniu ACL (pierwotny uraz), dzięki której operacja (drugi uraz) ma mniejsze powikłania.
Obecnie rozwój technik operacyjnych skoncentrowany jest na dążeniu do jak najkrótszej hospitalizacji pozabiegowej pacjenta, w celu uniknięcia niekorzystnych następstw ograniczenia codziennej aktywności ruchowej. Decyzja o rekonstrukcji ACL zależy od czynników takich jak:
-
stopień niestabilności kolana,
-
wiek pacjenta,
-
poziom odczuwanych przez pacjenta negatywnych wrażeń dotyczących stawu kolanowego,
-
nawracające uszkadzanie łąkotek,
-
obecność zjawiska ”uciekania kolana” pomimo próby leczenia zachowawczego.
Rehabilitacja
Bazując na dostępnej literaturze naukowej coraz częściej spotkać można się ze stwierdzeniem, że rehabilitacja jest równie ważna jak sama rekonstrukcja, by pacjenci wrócili do aktywności sprzed urazu. Obecnie naukowy świat fizjoterapii skupia się na zagadnieniu; jak wcześnie można przystąpić do rehabilitacji po operacji rekonstrukcji ACL. Niestety rozbieżności pojawiające się w tej kwestii sprawiają, że nie ma jeszcze standaryzowanego schematu postępowania. Nieścisłości występują także w przypadku zdań na temat stabilizacji pooperacyjnej stawu; kiedy powinno się otrzymać pełny ROM stawu kolanowego, kiedy stosować zamknięty (CKC), a kiedy otwarty łańcuch kinematyczny (OKC) w ćwiczeniach.
Ilości podejść i protokołów rehabilitacji jest tak wiele, jak wiele jest ośrodków rehabilitacyjnych, dlatego też brakuje wspólnego stanowiska. Jednakże cele, do których dąży się po rekonstrukcji ACL, w większości prac badawczych się pokrywają. Należą do nich:
-
zlikwidowanie obrzęku i bólu,
-
przywrócenie pełnego ROM i elastyczności stawu kolanowego,
-
wyeliminowanie zaniku mięśniowego,
-
normalizacja chodu,
-
powrót do pracy i codziennej aktywności pacjenta,
-
powrót siły i wytrzymałości mięśni jak sprzed urazu,
-
przywrócenie prawidłowej propriocepcji,
-
przywrócenie pewności siebie i przezwyciężenie lęku przed aktywnością fizyczną. Ten punkt jest celem szczególnie ważnym jeśli chodzi o leczenie sportowców.
Badania naukowe Saka T. nie wykazały szkodliwego wpływu przyspieszonej rehabilitacji, przez co pacjentom zaleca się obciążanie kończyny od razu po zabiegu, zginanie jej do 90 stopni oraz wykonywanie ćwiczeń w CKC (closed kinetic chain). Czynnikami świadczącymi o gotowości pacjenta do ćwiczeń w niestabilnych pozycjach, odbudowujących propriocepcję są przede wszystkim; brak dolegliwości bólowych oraz ustąpienie obrzęku stawu kolanowego. Ekscentryczne ćwiczenia mięśnia czworogłowego oraz izokinetyczne ćwiczenia mięśni tylnej grupy uda można bezpiecznie włączyć w plan rehabilitacji trzy tygodnie po zabiegu. Podkreśla się też pozytywne efekty pracy samodzielnej pacjenta w domu. Ćwiczenia w CKC prowadzi się do 6 tygodnia, a po tym okresie można wprowadzić ćwiczenia w OKC (open kinetic chain).
Wright i wsp. donoszą także, że wczesne obciążanie kończyny po rekonstrukcji ACL może mieć wpływ na zmniejszenie bólu w stawie rzepkowo-udowym. Na podstawie analizy literatury nie zaobserwowali oni znaczących korzyści płynących z stabilizowania pooperacyjnego stawu kolanowego w odniesieniu do grupy osób, u których takiej stabilizacji nie zastosowano.
Opracował
Maciej Stolarz
BIBLIOGRAFIA:
-
Kvist J., Kartus J., Karlsson J., Forssblad M. Results from the Swedish national anterior cruciate ligament register. Arthroscopy, 2014 Aug; 30(8):1044.
-
Levine J., Kiapour A., Quatman C., Wordeman S., Goel V., Hewett T., Demetropoulos C. Clinically Relevant Injury Patterns After an Anterior Cruciate Ligament Injury Provide Insight Into Injury Mechanisms. Am J Sports Med., 2013 February; 41(2): 385–395.
-
Sutton K., Bullock J. Anterior cruciate ligament rupture: differences between males and females. J Am Acad Orthop Surg., 2013 Jan; 21(1):41-50.
-
Swart E., Redler L., Fabricant PD., Mandelbaum BR., Ahmad CS., Wang YC. Prevention and screening programs for anterior cruciate ligament injuries
in young athletes: a cost-effectiveness analysis. J Bone Joint Surg Am.,
2014 May; 7;96(9):705-11. -
Hewett T., Myer G. The Mechanistic Connection Between the Trunk, Hip, Knee, and Anterior Cruciate Ligament Injury. Exerc. Sport Sci. Rev., 2011;39:4: 161-166.
-
Hashemi J., Breighner R., Chandrashekar N., Hardy D., Chaudhari A., Shultz S., Slauterbeck J., Beynnon B. Hip extension, knee flexion paradox: A new mechanism for non-contact ACL injury. Journal of Biomechanics, 2011; 44: 577–585.
-
Lin C., Liu H., Gros M., Weinhold P., Garrett W., Yu B. Biomechanical risk factors of non-contact ACL injuries: A stochastic biomechanical modeling study. Journal of Sport and Health Science, 2012; 1: 36-42.
-
Wild C., Steele J., Munro B. Why Do Girls Sustain More Anterior Cruciate Ligament Injuries Than Boys? A Review of the Changes in Estrogen and Musculoskeletal Structure and Function during Puberty. Sports Med., 2012; 42 (9): 733-749.
-
Shimokochi Y., Shultz S. Mechanisms of Noncontact Anterior Cruciate Ligament Injury. Journal of Athletic Training, 2008; 43(4):396–408.
-
McLean S., Beaulieu M. Complex Integrative Morphological and Mechanical Contributions to ACL Injury Risk. Exerc. Sport Sci. Rev., 2010;38(4): 192-200.
-
Georgoulis A., Ristanis S., Moraiti C., Paschos N., Zampeli F., Xergia S.,
Georgiou S., Patras K., Vasiliadis H., Mitsionis G. ACL injury and reconstruction: Clinical related in vivo biomechanics. Orthopaedics & Traumatology: Surgery & Research, 2010; 96S:119-S128. -
Strunick D., Van Gorder R., Vacek P., DeSarno M., Gardner-Morse M.,
Tourville T., Slauterbeck J., Jahnson R., Shultz S., Beynnon B. Tibial Articular Cartilage and Meniscus Geometries Combine to Influence Female Risk of Anterior Cruciate Ligament Injury. Wiley Online Library, 6 August 2014; DOI 10.1002/jor.22702. -
Dragoo J., Braun H., Durham J., Chen M., Harris A. Incidence and risk factors for injuries to the anterior cruciate ligament in National Collegiate Athletic Association football: data from the 2004-2005 through 2008-2009 National Collegiate Athletic Association Injury Surveillance System. Am J Sports Med., 2012; 40(5):990-5.
-
Wing Hung Alex Ng, James Francis Griffith, Esther Hiu Yee Hung, Bhawan Paunipagar, Billy Kan Yip Law, Patrick Shu Hang Yung. Imaging of the anterior cruciate ligament. World J Orthop., 2011;18, 2(8): 75-84.
-
Wheaton M., Jensen N. The ligament Injury Connection to Ostoarthritis. Journal of Prolotherapy, 2010; (2)1:294-304.
-
Farshad M., Gerber C., Meyer D., Schwab A., Blank P., Szucs T. Reconstruction versus conservative treatment after rupture of the anterior cruciate ligament: cost effectiveness analysis. BMC Health Services Research, 2011; 11:317.
-
Kiapour A., Murray M. Basic science of anterior cruciate ligament injury and repair. Bone Joint Res., 2014; 3:20–31.
-
Evans S., Shaginaw J., Bartolozzi A. ACL RECONSTRUCTION – IT’S ALL ABOUT TIMING. The International Journal of Sports Physical Therapy, 2014;9(2): 268.
-
Pereira M., Vieira N., Brandao R., Ruaro J., Grignet R., Frez A. Physiotherapy after reconstruction of anterior cruciate ligament. Acta Ortop Bras., 2012; 20(6):372-5.
-
Kruse L., Gray B., Wright R. Rehabilitation After Anterior Cruciate Ligament Reconstruction. J Bone Joint Surg Am., 2012; 94:1737-48.
-
Saka T. Principles of postoperative anterior cruciate ligament rehabilitation. World J Orthop., 2014 September; 18; 5(4): 450-459.
-
Wright R., Preston E., Fleming B., Amendola A., Andrish J., Bergfeld J., Dunn W., Kaeding C., Khun J., Marx R., McCarty E., Parker R., Spindler K., Wolcott M., Wolf B., Williams G. ACL Reconstruction Rehabilitation: A Systematic Review Part II. J Knee Surg., 2008; 21(3): 225–234.
-
Norouzi S., Esfandiarpour F., Shakourirad A., Salehi R., Akbar M., Farahmand F. Rehabilitation after ACL Injury: A Fluoroscopic Study on the Effects of Type of Exercise on the Knee Sagittal Plane Arthrokinematics. BioMed Research International, 2013, Article ID 248525.
-
Koga H., Nakamae A., Shima Y., Iwasa J., Myklebust G., i wsp. Knee Joint Kinematics in 10 Injury Situations From FemaleTeam Handball and Basketball. AJSM PreView, published on July 1, 2010 as doi:10.1177/0363546510373570